Ischämischer Schlaganfall und Transitorische ischämische Attacke (TIA)
Prähospitalisationsphase
Patienten müssen an Ort und Stelle und ohne Zeitverlust klinisch mithilfe geeigneter Scores (mit hoher Sensitivität) eingeschätzt und im Hinblick auf eine akute Intervention gescreent werden. Am bekanntesten ist die Cincinnati Prehospital Stroke Scale (CPSS), die in Aufklärungskampagnen verbreitet und instruiert werden kann. Diese erfasst allerdings nur die Sprache und Motorik. Eher auf den Notarztdienst zugeschnitten ist die Los Angeles Paramedic Stroke Scale (LAPSS)[1]. Für Laien eignet sich der FAST-Test gut. Grundsätzlich eignet sich das Kriterium eines akut aufgetretenen fokalen neurologischen Defizits (u.a. Sprache, Motorik, Sehstörung, schwerer Schwindel) gut für den Entscheid, ob ein Schlaganfall vorliegt. Aufgrund der Behandlungsoption der endovaskulären Therapie, welches nur in Stroke Centers verfügbar ist, sollte durch den Rettungsdienst auch die Wahrscheinlichkeit eines proximalen Gefässverschlusses (LVO = large vessel occlusion) beurteilt werden. Hierfür schlägt die Schweiz. Hirnschlaggesellschaft die RACE-Scale als Instrument vor, die in diesem Setting validiert ist.
FAST – Face, Arm, Speech (Abnormalities) and Telephone
| Ja | Nein | |
| 1. Gesichtslähmung (Face) | ☐ | ☐ |
| 2. Einseitige Armschwäche (Arm) | ☐ | ☐ |
| 3. Abnorme Sprache (Speech) | ☐ | ☐ |
| 4. Telefonische Benachrichtigung Notfalldienst (Telephone) |
Weitere Kriterien, die einen Schlaganfall wahrscheinlicher machen
- Alter > 45 Jahre
- Kein Anfallsleiden in der Anamnese
- Auftreten der neurologischen Symptome in den letzten 24 Std. Genauer Beginn der Symptomatik (Zeugen?)
- Patient funktionell körperlich und mental unabhängig vor dem Ereignis
- Blutglukose zwischen 3.3 und 22 mmol/l
Falls alle drei Kriterien der CPSS erfüllt sind, liegt mit grosser Wahrscheinlichkeit eine Ischämie im vorderen Stromgebiet einer Hemisphäre vor. Dieser «Face/Arm/Speech»-Test hat bei einem positiven Hauptkriterium eine Sensitivität von ca. 90% für das Erkennen einer Ischämie im Mediastromgebiet. Schlechter ist die Sensitivität für das Erkennen einer Ischämie im Posteriorstromgebiet resp. im Hirnstamm (z.B. Basilaristhrombose).
Nach der initialen Einschätzung
Bei Verdacht auf Schlaganfall niederschwellig zuweisen, Zielspital anrufen, das einen Akutbehandlungsauftrag im Rahmen eines Schlaganfallnetzwerkes hat (KSSG 071 494 11 11, diensthabenden Neurologen verlangen, interne Nummer 9420) und als Schlaganfall-Notfall anmelden. Patiententransport via Sanitätsnotruf 144 oder REGA 1414 anfordern. Fahrt ins Spital mit Sondersignal bei Symptombeginn innerhalb der letzten 24 Stunden.
- Bei einer Entfernung des Ereignisses zum Stroke Center < 20 Minuten sollte das Stroke Center direkt angefahren werden, unabhängig von der Wahrscheinlichkeit eines LVO (= large vessel occlusion).
- Falls der Weg zur Stroke Unit kürzer ist als zum Stroke Center, scheint das Drip & Ship Konzept (systemische Thrombolyse im nächstgelegenen Spital mit Behandlungsauftrag, sekundärer Transport bei LVO ins Zentrum) ab einer Transportzeit von > 20 Minuten zwischen den beiden Institutionen Sinn zu ergeben.
- Fahrtwege weg vom Stroke Center und hin zu einer Stroke Unit von mehr als 10 min. sollten vermieden werden, da dieser Weg bei Verlegung ins Stroke Center nochmals gemacht werden muss.
Massnahmen beschränken
- Sicherung der Vitalfunktionen
- Glukosegabe bei Hypoglykämie
- Wenn möglich grosslumigen venösen Zugang kubital anlegen ≤ 17 G (weiss, grau oder orange)
Unterlassen
- Keine Antithrombotika (z.B. Aspirin, Heparin und ähnliche) geben (ischämischer und hämorrhagischer Infarkt können initial klinisch nicht unterschieden werden)
- In der Regel keine antihypertensive Behandlung (nur wenn > 220/120 mmHg)
Beachten
Schlaganfälle können auch im Alter < 45 Jahre auftreten, selbst im Kindesalter.
Keine Vorabklärungen in Institutionen durchführen, die keinen Akutbehandlungsauftrag haben.
Wenn möglich Begleitperson aus der Familie für Fremdanamnese und allfällig notwendige Entscheidungsfindung mitschicken oder zumindest eine Telefonnummer für Rückfragen notieren.
Wenn möglich den Ereigniszeitpunkt eruieren (oder den zuletzt symptomfreien Zeitpunkt).
Akutbehandlung des ischämischen Schlaganfalles
Indikationskriterien für eine intravenöse Thrombolyse oder eine endovaskuläre Revaskularisation
- Klinische Diagnose eines ischämischen Schlaganfalls
- Ausschluss einer akuten intrakraniellen Blutung im CT oder MRI
- Behinderndes Defizit zum Zeitpunkt der Untersuchung (in der Regel: NIHSS-Score ≥ 4 Punkte) u/o Aphasie u/o Hemianopsie
- Intervall zwischen Symptom- und Therapiebeginn 0–4.5 Std. für die intravenöse und 0–8 Std. für die endovaskuläre Behandlung
- Bei Symptombeginn < 24 Std. (inclusive «last seen well» < 24 Std.), Nachweis eines proximalen Gefässverschlusses sowie vorhandener Penumbra (CT- oder MRI basiert): endovaskuläre Behandlung
- Bei Wake-up-Konstellation oder unklarem zeitlichen Beginn ohne Nachweis eines proximalen Gefässverschlusses, aber mit vorhandener Penumbra (MRI-/CT basiert), intravenöse Thrombolyse
Kontraindikationen für eine intravenöse oder intraarterielle Thrombolyse können unter www.guidelines.ch nachgesehen werden und werden in der behandelnden Klinik überprüft. Viele dieser Kriterien sind relativ. Das Ziel sollte in jedem Fall sein, möglichst eine Behandlung durchzuführen, sofern nicht klare Gründe dagegen sprechen.
Merkpunkte
- Die systemische Thrombolyse (mit rt-PA) verbessert das Outcome beim akuten ischämischen Hirninfarkt.
- Bei proximalen Gefässverschlüssen bringt die Kombination der systemischen Thrombolyse mit einer endovaskulären Revaskularisation (Bridging) einen klaren Zusatznutzen.
- Ob allein oder in Kombination ist der Nutzen der Interventionen stark zeitabhängig. Zeitvorgaben: «Door to needle»: 30 Min. bzw. «Door to groin puncture»: 60 Min.
- Die Einnahme von Aspirin und/oder Clopidogrel kontraindizieren die Thrombolyse nicht. Bei Kombination beider Substanzen muss aber mit einer erhöhten Blutungsrate gerechnet werden.
- Bei therapeutischer, oraler Antikoagulation mit einem Vit. K-Antagonisten (INR > 1.7) oder einem NOAK kann bei akutem Verschluss eines proximalen Gefässes mittels endovaskulärer Revaskularisation behandelt werden.
- Ein fortgeschrittenes Alter (> 80 Jahre) ist kein Ausschlusskriterium für eine Behandlung.
- Nach Thrombolyse/endovaskulärer Revaskularisation: keine Gabe von Antiaggregantien/Antikoagulantien während 24 Std. bis zur Durchführung einer zerebralen Bildgebung zum Ausschluss einer relevanten Einblutung. Ausnahmen sind besondere Umstände, wie einer Dissektion, akutem Stenting extra- und intrakraniell (individueller Entscheid).
- Falls keine Thrombolyse möglich ist, soll die mechanische Thrombektomie als alleinige Akuttherapie erwogen werden.
- Wenn keine Thrombolyse und keine endovaskuläre Revaskularisation möglich ist (Kontraindikation, Zeitfenster überschritten etc.) Gabe von 250 mg Aspirin iv (alternativ 300 mg po) und Thromboseprophylaxe mit niedermolekularem Heparin sc, nach der Durchführung einer zerebralen Bildgebung zum Blutungsausschluss.
- Bestehen Hinweise auf eine kardiale Embolie wird 24 Std. postinterventionell mit intravenösem Heparin begonnen, initial mit 10’000 E/24h. Im Verlauf erfolgt abhängig von der Infarktgrösse[2] eine therapeutische Antikoagulation. Ein früherer Beginn wird aktuell in mehreren grossen Studien untersucht.
- Die akute (revaskularisierende) Schlaganfallakutbehandlung (mechanische Thrombektomie/systemische Thrombolyse) ist bis 24 Std. nach Symptombeginn respektive bei Wake up stroke möglich. Die Triage muss in einem dafür qualifizierten Spital (Stroke Unit, Stroke Center) erfolgen.
- Eine signifikante neurologische Besserung mit sekundärer Verschlechterung ist in der Akutsituation möglich, weshalb eine kontinuierliche Überwachung über mindestens 24 Std. indiziert ist.
Probleme in der akuten und postakuten Phase
In der akuten bzw. postakuten Phase können spezifische neurologische und internistische Probleme zu lebensbedrohlichen Komplikationen führen oder durch Interaktion mit der zerebrovaskulären Reserve das neurologische Outcome beeinträchtigen. Entsprechend ist die Betreuung des akuten Schlaganfallpatienten durch ein erfahrenes Behandlungsteam (Stroke Unit) mit einem besseren Outcome assoziiert.
Dysphagie nach Schlaganfall
- Schluckstörungen nach Schlaganfall sind häufig (bis 50%).
- Wegen des Aspirationsrisikos und des Risikos der Mangelernährung muss systematisch nach einer Schluckstörung gesucht (Dysphagiescreening) und allenfalls therapeutische Schritte eingeleitet werden. Nähere Informationen unter: www.guidelines.ch
Masseneffekt durch malignes Hirnödem[3]
Indikation für frühzeitige (24–48 Std.) parieto-temporale Schädeldekompression bei malignem Mediainfarkt:
- Alter < 60 (–70) Jahre
- Symptombeginn vor < 24 Std. (in Ausnahmefällen auch später)
- Im CT oder MRI Infarktzeichen, die mindestens die Hälfte des Mediastromgebietes umfassen
- Mutmasslicher Wille des Patienten für ein aktives Vorgehen
- Keine Kontraindikationen für eine Operation
- Ein erfolgloser Rekanalisationsversuch bzw. erfolglose Thrombolyse ist ein weiteres Argument für eine Hemikraniektomie
Indikation für okzipitale Schädeldekompression bei Kleinhirninfarkt, meist ergänzt durch externe Ventrikeldrainage (EVD):
- Zeichen einer progressiven Druckerhöhung im Hirnstammbereich
- Radiologisch sichtbare Raumforderung
- Mutmasslicher Wille des Patienten für ein aktives Vorgehen
- Keine Kontraindikationen für eine Operation
Probleme, welche die zerebrovaskuläre Reserve beeinträchtigen können
- Hochgradige Stenose der A. carotis interna
- Arterielle Hypertonie und Hypotonie
- Tachy- und Bradyarrhythmie, meist i.R. eines Vorhofflimmerns
Seltene Probleme
- Zentrale Apnoe und Hypopnoe bei medullären Infarkten
- Behandlungsbedürftiges obstruktives Schlafapnoesyndrom
Internistische Probleme in der akuten und postakuten Phase
- Bei Temp. > 38.0 °C (tympanal) antipyretische Therapie (physikalisch, medikamentös [Paracetamol oder Metamizol]) einsetzen. Fokussuche (Anamnese, Blutkulturen, Thorax-Röntgenbild [Aspirationspneumonie?], Urinstatus), damit bei bakteriellem Infekt eine gezielte antibiotische Therapie zeitnah begonnen werden kann.
- Grundinfusion NaCl 0.9% oder Ringerlactat. Hypotone Infusionslösungen wie z.B. Glukose 5% vermeiden (Cave: Hirnödem).
- Thromboembolieprophylaxe: bei eingeschränkter Mobilität (und fehlenden Kontraindikationen) Gabe von niedermolekularem Heparin sc in prophylaktischer Dosierung. Bei Kontraindikationen intermittierende pneumatische Kompression der Beine.
- Blutzucker: engmaschige Kontrolle (Blutzuckertagesprofil) und Nüchtern-Werte zwischen 5.5 und 10.0 mmol/l anstreben.
- Rasche Wiederaufnahme der enteralen Ernährung (bei Thrombolyse frühestens am nächsten Tag), bei Dysphagie mittels nasogastraler Sonde. Parenterale Ernährung nur in Ausnahmefällen.
- Sauerstoffgabe: Sauerstoffsättigungs-Ziel > 92%.
- Blutdruck: Vor Beginn der Thrombolyse sind Werte von 185/110 mmHg, in den ersten 24 Stunden danach ≤ 180/105 mmHg anzustreben, aber schnelle Blutdruckabfälle um > 20% des Ausgangswertes zu vermeiden. Ohne medikamentöse oder mechanische Rekanalisation wird eine akute Behandlungsbedürftigkeit erst bei persistierenden Werten > 200/120 mmHg resp. Organmanifestationen (kardiale Ischämie, Herzinsuffzienz, Aortendissektion, hypertensive Enzephalopathie, Eklampsie) angenommen. Vorsichtiger (Wieder-) Beginn der antihypertensiven Therapie nach 24- 72 Std.
- Die Blutdruckuntergrenze richtet sich nach dem klinischen Bild, als Faustregel gilt > 120 mmHg systolisch. Symptomatische Hypotonien primär mit Volumengabe (NaCl 0.9% iv) behandeln.
Transitorische Ischämische Attacke (TIA)
Die transitorische ischämische Attacke (TIA) wird heute als neurologischer Notfall angesehen, da das Risiko, einen schweren Schlaganfall zu erleiden innerhalb der ersten 48 Std. bei bis zu 12% liegt. Deshalb müssen unter den TIA-Patienten die Hochrisiko-Patienten rasch identifiziert werden. Als solche gelten alle mit einem ABCD3– resp. ABCD3-I-Score von 4 Punkten und mehr. Dabei beinhaltet der bessere und bei uns angewendete ABCD3-I-Score zusätzlich den möglichen Nachweis einer ipsilateralen Stenose von mehr als 50% (CTA oder Doppler-/Duplexsonografie) und einer DWI-Läsion. Abhängig von der Einschätzung des Rezidivrisikos und der Latenz nach der TIA, der Risikokonstellation und den lokal verfügbaren Ressourcen soll der Entscheid für eine rasche ambulante oder stationäre Abklärung gefällt werden. Durch eine rasche Abklärung und Behandlung können ca. 80% der Rezidive verhindert werden.
Risikoeinschätzung anhand des ABCD3– und ABCD3-I-Score
| ABCD3-Score | ABCD3-I-Score | ||
| Alter | ≥ 60 Jahre | 1 | 1 |
| Blutdruck | ≥ 140/90 mmHg | 1 | 1 |
| Klinische Faktoren |
Sprachstörung ohne halbseitige Schwäche Halbseitige Schwäche |
1
2 |
1
2 |
| Dauer | 10–59 Minuten
≥ 60 Minuten |
1
2 |
1
2 |
| Diabetes mellitus | 1 | 1 | |
| Vorangegangene TIA in den letzten 7 Tagen | 1 | 2 | |
| Ipsilaterale ≥ 50%ige Stenose der A. carotis interna | NA | 2 | |
| DWI-Läsion im MRT | NA | 2 | |
| Summe | 0–9 | 0–13 |
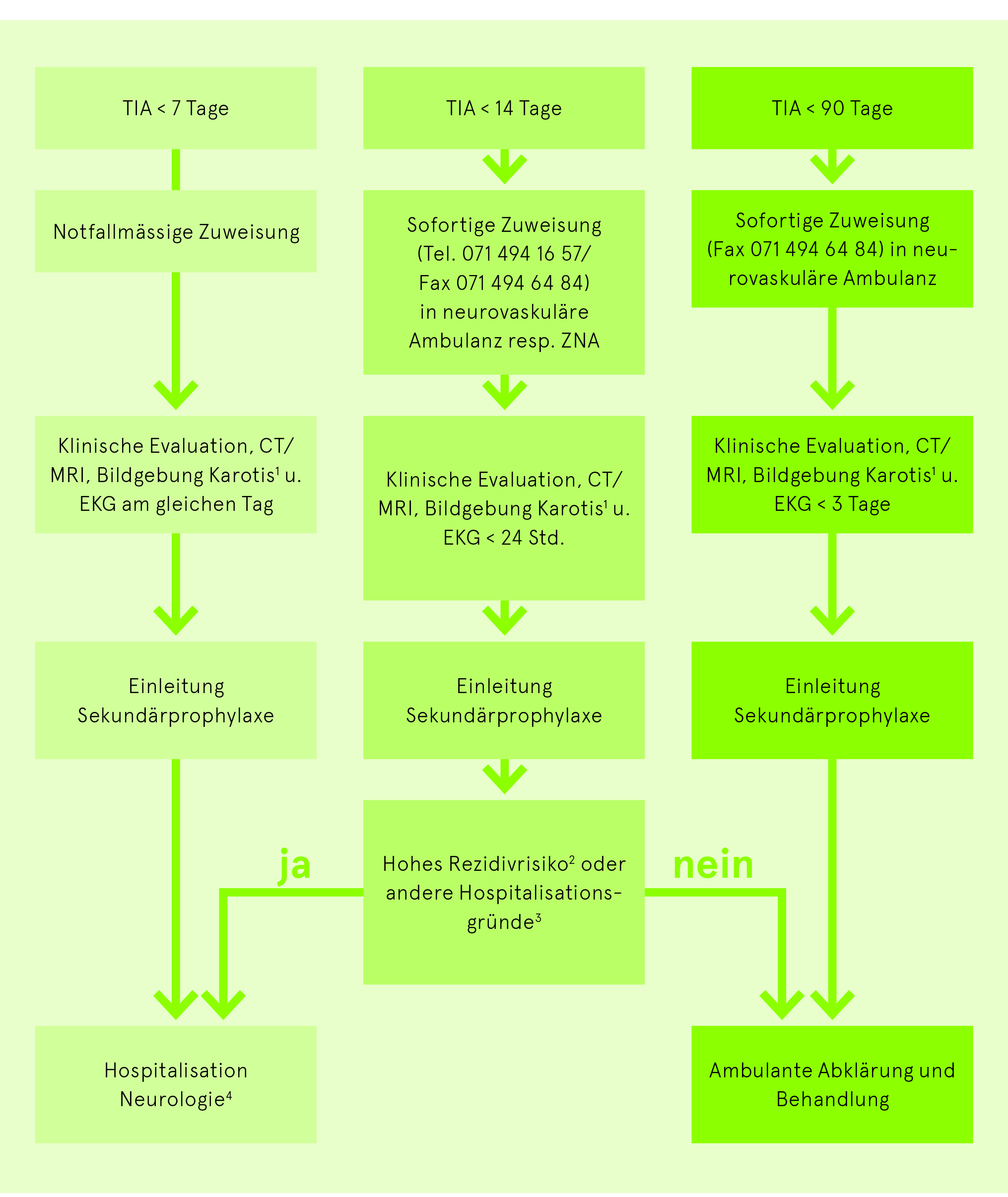
2 ABCD3 resp. ABCD3-I-Score > 4 Punkte
3 Co-Morbiditäten beachten wie Herzinsuffizienz, instabile Angina pectoris
4 Der Entscheid, ob der Patient auf die NIPS aufgenommen wird, kann der entsprechenden Indikationsliste entnommen werden. Bei TIAs sind dies: ABCD3 resp. ABCD3-I-Score > 4 Punkte, Vorhofflimmern, andere schwere Co-Morbiditäten
Sekundärprävention nach Schlaganfall/TIA
Pharmakotherapie
Antithrombotische Behandlung
- In der Regel Aspirin 300 mg/Tag für 7 Tage, danach 100 mg/Tag
- Bei TIA oder leichtem Schlaganfall (NIHSS ≤ 5) vorübergehend (ca. 2 Wochen) duale Thrombozytenaggregationshemmung mit Aspirin 100 mg/Tag + Clopidogrel 75 mg/Tag (initiale Aufsättigungsdosis Clopidogrel: 300mg)
- In ausgewählten Fällen mit sehr hohem Schlaganfallrezidivrisiko (hochgradige intra-/extrakranielle Stenose, ulzerierte Plaque, positives Embolie-Monitoring in der Dopplersonografie unter Aspirin): Aspirin 100 mg/Tag + Clopidogrel 75 mg/Tag (initiale Aufsättigungsdosis Clopidogrel 300mg) für maximal 3 Monate
- Extrakranielle Gefässdissektion (3–6 Monate): Aspirin 100 mg/Tag oder orale Antikoagulation mit Phenprocoumon (Marcoumar [Ziel-INR 2–3])
- Eine doppelte Thrombozytenaggregationshemmung von > 3 Monaten ist aus rein neurologischer Sicht nicht indiziert, da das Blutungsrisiko den sekundärprophylaktischen Nutzen überwiegt.
- Bei Therapieversagen Wirksamkeit der Thrombozytenaggregationshemmer durch den Multiplate-Test in vitro prüfen.
Behandlung mit Antikoagulantien
Indikation zur oralen Antikoagulation (OAK)[4]:
- Kardiale Emboliequelle:
- Vorhofflimmern: siehe entsprechendes Kapitel Seite
- «Klassifizierung: valvulär vs nicht-valvulär» siehe Seite
- Valvuläres Vorhofflimmern[5]: siehe «Therapie der Mitralklappenstenose» Seite
- Nicht-valvuläres Vorhofflimmern: gemäss «CHA2DS2-VASc Score» Seite und «HAS-BLED Score» Seite
- Bei Vorhofflimmern und Koronarer Herzkrankheit: siehe «Vorgehen bei Indikation für Thrombozytenaggregationshemmer und OAK» Seite
- Mechanische und biologische Herzklappen[6]: siehe Kapitel Valvuläre Herzerkrankung «Follow-up bei Klappenerkrankungen» Seite.
- Linksventrikulärer Thrombus: Vitamin K-Antagonist (i.d.R. Phenprocoumon [Marcoumar] Ziel-INR: 2–3) oder ggf. NOAK für mind. 3 Monate[7]
- Akutes Koronarsyndrom mit Herzwandaneurysma mit/ohne Nachweis eines linksventr. Thrombus: siehe Kapitel ACS «Antithrombotische Therapie bei PCI und Indikation einer OAK» Seite in Rücksprache mit dem behandelnden Kardiologen
- Vorhofflimmern: siehe entsprechendes Kapitel Seite
- Sinus-/Hirnvenenthrombose: Vitamin K-Antagonist (i.d.R. Phenprocoumon [Marcoumar] mit Ziel-INR: 2–3) für 3-6 Monate
Empfehlungen für die Behandlung der arteriellen Hypertonie
- Blutdruck-Ziel < 140/80 mmHg, bei Jüngeren (< 65-jährig) evtl. < 130/80 mmHg (nicht < 120 mmHg), falls gut toleriert.
- ACE-Hemmer in Kombination mit thiazidähnlichen Diuretika sind erste Wahl. Alternativ Kalziumantagonisten und Angiotensin-Rezeptor-Blocker. Keine Kombination von ACE-Hemmern, Angiotensin-Rezeptor-Blocker und Reninhemmern. Betablocker gehören in dieser Situation nicht zu den Antihypertensiva der ersten Wahl. Die Auswahl des Medikamentes muss den Begleiterkrankungen (KHK, PAVK, Diabetes mellitus, Niereninsuffizienz) angepasst werden.
- Gewichtsreduktion, körperliches Training, salzarme Ernährung und Einschränkung des Alkoholkonsums helfen bei der Blutdrucksenkung und sollten die medikamentöse Therapie ergänzen.
Empfehlungen für die medikamentöse Lipidsenkung
- Bei Patienten mit ischämischem Hirninfarkt ist eine Therapie mit einem potenten Lipidsenker (Statin) unabhängig von den Ausgangswerten indiziert. Zielwert LDL < 1.8 mmol/l
Hochgradige Karotisstenose
- Bei hochgradigen, symptomatischen Karotisstenosen (> 70% [distaler Stenosegrad/NASCET]) ist ein Stenting oder eine Endarteriektomie indiziert.
- Der Nutzen der invasiven Therapie nimmt mit progredientem Stenosegrad zu. Er ist geringer bei einem Stenosegrad zwischen 50 und 70%, bei Frauen und wenn der Eingriff mehr als 12. Woche nach dem Ereignis durchgeführt wird.
- Der Zeitraum zwischen Ereignis und invasiver Therapie sollte mit Thrombozytenaggregationshemmern überbrückt werden. Ist eine Stenose unter einem Thrombozytenaggregationshemmer symptomatisch geworden, empfiehlt sich die Kombination von Aspirin 100 mg/Tag mit Clopidogrel 75 mg/Tag bis zur Operation. Danach Aspirin 100 mg/Tag. Zudem sollte bis zum Eingriff ein hochpotentes und hochdosiertes Statin (z.B. Atorvastatin 80 mg/Tag) verabreicht werden. Wird primär ein Stenting erwogen, soll mindestens eine Woche vorher eine Kombination von Aspirin 100 mg/Tag mit Clopidogrel 75 mg/Tag durchgeführt und das Ansprechen 1 Tag vor dem Eingriff mittels Multiplate-Tests überprüft werden.
- Die Karotisangioplastie mit Stenteinlage hat im Vergleich zur operativen Therapie in Bezug auf das periprozedurale Risiko bei der Behandlung symptomatischer Karotisstenosen ein leicht erhöhtes Kurzzeitrisiko (insbesondere bei Patienten > 70 Jahre).
- Bei unter 70-Jährigen ist das periprozedurale Risiko des Stentings vergleichbar mit demjenigen der Endarterektomie.
- Die Langzeitergebnisse (10 Jahre) bezüglich Schlaganfall und Restenoserate sind für beide Verfahren vergleichbar.
- Die Karotisendarterektomie ist derzeit die Therapie der ersten Wahl bei Patienten über 70 Jahre. Bis 70 Jahre sind beide Verfahren als gleichwertig einzustufen. Ein Stenting ist Therapie der Wahl bei Patienten mit Rezidivstenose nach TEA, hochgradiger Stenose nach Strahlentherapie oder hoch sitzender und einer chirurgischen Intervention schwer zugänglichen Stenose sowie bei Hochrisikopatienten.
Persistierendes Foramen ovale, PFO
PFO-Verschluss
Die Empfehlung für/gegen einen PFO-Verschluss ist stets ein individueller Entscheid im interdisziplinären PFO-Kolloquium und nach sorgfältiger ätiologischer Abklärung:
- MRI Neurokranium: Infarktmuster embolisch versus lakunär?
- Darstellung der hirnversorgenden Gefässe (CT-Angiografie und/oder MR-Angiografie und/oder Doppler/Duplexsonografie der extrakraniellen hirnversorgenden Gefässe)
- Transthorakale Echokardiografie: Insbesondere bei < 60-Jährigen ohne klare Ätiologie und embolischem Infarktmuster zur Suche nach einem möglichen Rechts-Links-Shunt (insbesondere PFO); bei unklarem Befund transkranieller Doppler («Bubble-Test»)
- 7d-Holter-EKG (30d-Holter bzw. implantierbarer Rhythmusrecorder bei entsprechendem Risikoprofil siehe Richtlinien Neurologie KSSG www.guidelines.ch)
Entscheidungsbaum PFO-Verschluss
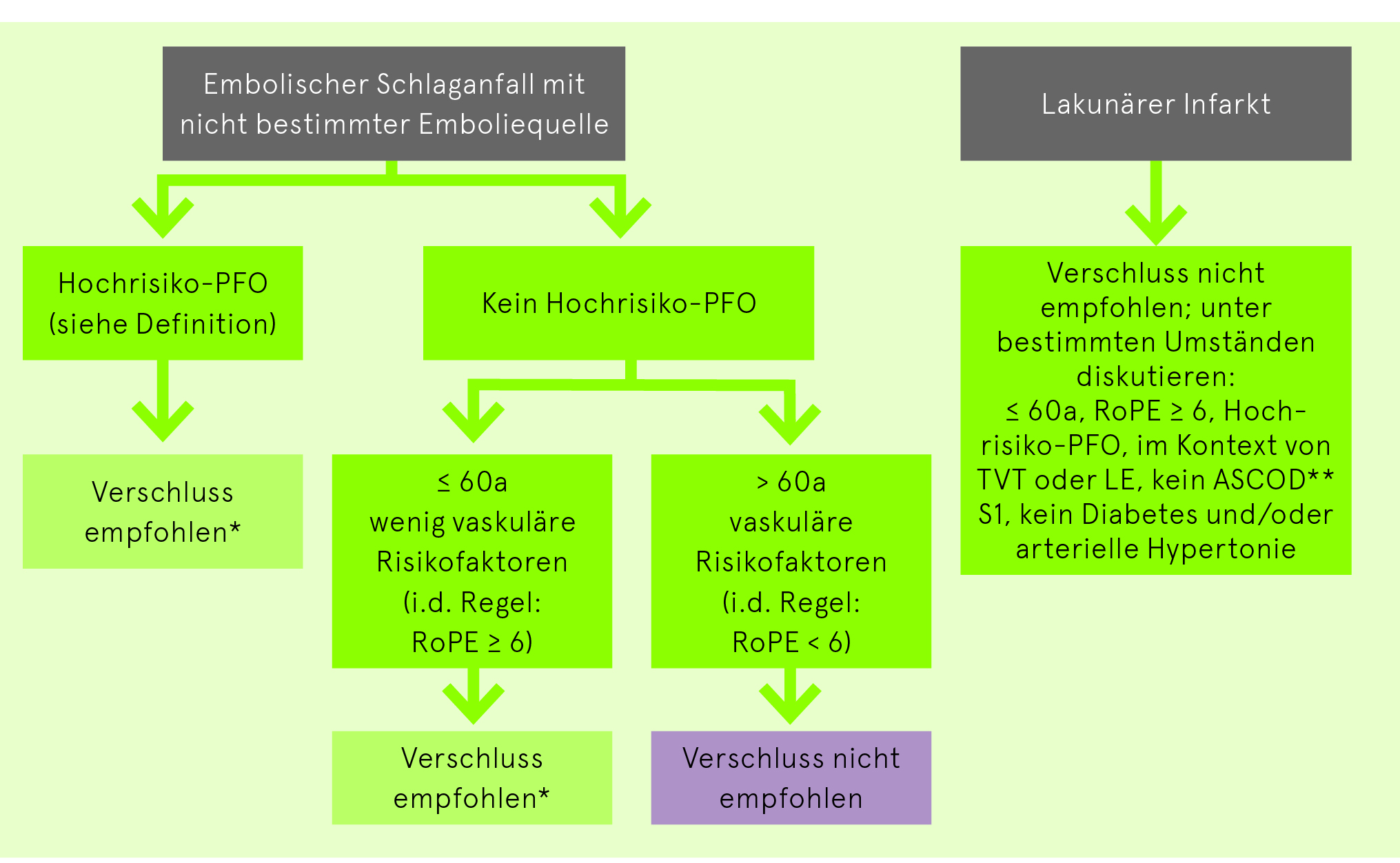
**ASCOD = Phänotypisierung des ischämischen Schlaganfalles (A: Makroangiopathie, S: Mikroangiopathie, C: kardiale Pathologie, O: andere Ursachen, D: Dissektion (Amarenco, et al. Cerebrovasc Dis 2013;36:1-5)
Folgende Kriterien in der Echokardiografie sprechen für eine Hochrisikokonstellation («Hochrisiko-PFO»):
- Hypermobiles interatriales Septum ≥ 10mm / ASA ≥ 10(15) mm
- Grosser Rechts-Links-Shunt (Übertritt > 30 Microbubbles innerhalb von 3 Herzzyklen)
- PFO-Durchmesser ≥ 2 mm
- Ausgeprägte Eustachische Klappe oder Chiari-Netzwerk
Der RoPE-Score erlaubt es, bei Patienten mit ätiologisch ungeklärtem Schlaganfall und PFO die Wahrscheinlichkeit eines inzidentellen versus eines pathogenen PFO abzuschätzen. Grundsätzlich gilt, dass ein RoPE-Score von ≥ 6 auf ein pathogenes PFO hinweisend ist.
| RoPE-Score | Punkte |
| Keine arterielle Hypertonie | 1 |
| Kein Diabetes | 1 |
| Kein(e) Stroke/TIA in der Vorgeschichte | 1 |
| Nichtraucher | 1 |
| Kortikaler Infarkt (CT/MRI) | 1 |
| Alter 18–29 Jahre | 5 |
| Alter 30–39 Jahre | 4 |
| Alter 40–49 Jahre | 3 |
| Alter 50–59 Jahre | 2 |
| Alter 60–69 Jahre | 1 |
| Alter ≥ 70 Jahre | 0 |
| Total | 10 |
Medikamentöse Behandlung nach interventionellem PFO-Verschluss mittels Device [8]
- Vaskuläre Risikofaktoren sind unabhängig von einem etwaigen PFO-Verschluss gemäss der üblichen Risikostratifizierung zu therapieren.
- Eine gerinnungshemmende Therapie mit einem Thrombozytenaggregationshemmer ist in der Regel unabhängig vom Entscheid für einen PFO-Verschluss dauerhaft indiziert (als Einzelfallentscheid ggf. alternativ OAK (NOAK), insb. wenn kein Verschluss und/oder bei Rezidiv).
- Nach einem PFO-Verschluss bedarf es einer mindestens dreimonatigen dualen Thrombozytenaggregationshemmung.
- Bei Verschluss mittels Device ist eine Endokarditis-Prophylaxe (orange) für 6 Monate nach PFO-Verschluss zwingend indiziert.
Periinterventionelles Management bei Patienten nach ischämischem Schlaganfall unter oraler Antikoagulation (OAK)
- Siehe Kapitel «Periinterventionelles Management unter gerinnungshemmender Medikation» Seite
Quellen/Links
- www.strokeunit.kssg.ch
- www.guidelines.ch (Richtlinien Ostschweizer Schlaganfallnetzwerk)
- www.neurovasc.ch
- www.eso-stroke.org
- www.awmf.org/leitlinien/aktuelle-leitlinien/ll-liste/deutsche-schlaganfall-gesellschaft-dsg.html
- www.stroke.org
PD Dr. Georg Kägi
Dr. Markus Diethelm
Dr. Christian Gall
Dr. Gian-Reto Kleger
Dr. Bruno Minotti
Dr. Jochen Vehoff
Dr. Daniel Weilenmann
- Das modifizierte LAPSS-Formular kann von der Website des Schlaganfallzentrums heruntergeladen werden: www.strokeunit.kssg.ch ↵
- Zeit bis Beginn OAK: TIA: sofort; kleiner Infarkt: 3–5 Tage; mittelgrosser Infarkt: 5–7 Tage; grosser Infarkt: 14 Tage ↵
- Empfehlungen der schweizerischen Arbeitsgruppe: International Journal of Stroke 2009; 4:218–223 ↵
- Bei akutem Territorialinfarkt volle Antikoagulation nur in Ausnahmefällen (Gefässdissektion, Sinus-/Hirnvenenthrombose, linksventr. Thrombus, flottierender Thrombus in der ACI) zu erwägen. Ansonsten in den ersten 7 Tagen keine therapeutische Verlängerung der PTT/PiCT anstreben. ↵
- NOAKs sind bei valvulärem Vorhofflimmern kontraindiziert. ↵
- NOAKs sind bei mechanischen Klappen kontraindiziert. Bei ischämischem Schlaganfall/TIA trotz adäquater OAK, Zugabe von 100 mg Aspirin/Tag, falls kein hohes Blutungsrisiko vorliegt. ↵
- Dauer abhängig vom echokardiografischen Verlauf ↵
- Prozedere wird im KSSG im Rahmen des interdisziplinären PFO-Kolloquiums festgelegt ↵